Was sind sporenbildende Probiotika – und wie helfen Sporenbildner Deinem Darm?
Wenn es Dir um die Förderung Deiner Darmgesundheit geht, dann hast Du sicherlich schon von Probiotika gehört – lebenden Mikroorganismen, die auch in deinem Darm vorkommen und dessen Einnahme in ausreichend hohen Dosen deine Darmflora unterstützen soll. Wusstest Du, dass es viele unterschiedliche Arten von Probiotika gibt und sie alle Unterschiede aufweisen? In unserem Probiotika Guide haben wir Dir die Unterschiede bereits erklärt – hier hingegen geht es um eine ganz spezielle Gruppe im Detail: die sporenbildenden Probiotika. Im Gegensatz zu vielen anderen klassischen Probiotika sollen diese nämlich besser im Magen überleben können – die Hürde, an der viele Bakterien scheitern. Deshalb geht es heute genau um diese Mechanismen und die potenziellen Vorteile von Sporenbildnern.
Übrigens: Wir recherchieren und schreiben unsere Artikel in Zeiten künstlicher Intelligenz noch selbst – das erkennst Du auch an den vielen wissenschaftlichen Referenzen im und am Ende dieses Beitrags. Nur so können wir unserem eigenen Qualitätsanspruch gerecht werden. Wir wünschen viel Spaß beim Lesen!
Was sind sporenbildende Probiotika?
Probiotika sind keineswegs eine einheitliche Gruppe von Bakterien. Vermutlich kennst Du die klassischen Lactobacillus- und Bifidobacterium-Stämme, die sich in fast jedem Produkt befinden. Diese sind aktive Bakterien ohne besondere Schutzhülle, die in Deinem Darm Teil der normalen Darmflora sind. Das Ziel mit der Gabe dieser Bakterien ist, die Magensäure zu überwinden, sich im Darm anzusiedeln und die Darmflora damit anzureichern. Was wir mittlerweile jedoch wissen: Dies findet nur begrenzt statt; ein großer Teil der zugeführten Probiotika befindet sich nur vorübergehend im Darm – sie siedeln sich aber nicht an. Zudem sind diese Bakterien wie erwähnt von vornherein aktiv und angreifbar; deshalb ist unklar, wie viele tatsächlich den Magen und die Magensäure überleben.
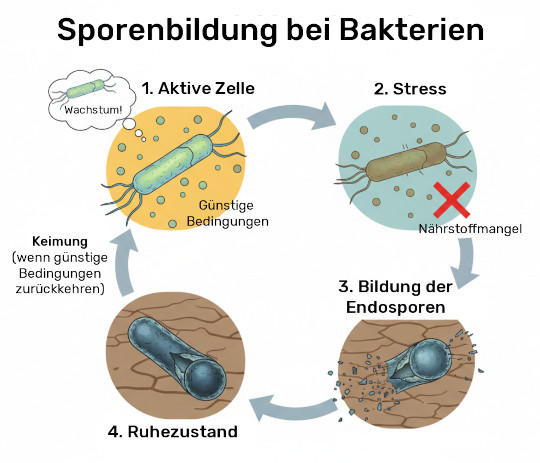
Sporen-Probiotika hingegen besitzen einen sogenannten Schutzmantel, weil sie unter ungünstigen Bedingungen aus ihrem aktiven Zustand sogenannte Endosporen bilden können: Das Bakterium strukturiert sich um, bildet einen besonders widerstandsfähigen Schutzmantel und geht – wenn wir so möchten – in eine Art „Winterschlaf“. Wenn die Endospore wieder von besseren Konditionen umgeben ist, kann sie erneut keimen – beispielsweise im Dünndarm nach Durchlaufen des Magens und der dort enthaltenen Säure. Diesen Überlebensvorteil wollen wir uns also genauer angucken, um den entscheidenden Unterschied von Sporen zu aktiven Bakterien zu verstehen.

Magensaftresistente Probiotika – Sporenbildner als Überlebenskünstler
Im Vergleich zu klassischen Probiotika wird postuliert, dass Sporenbildner gegenüber so gut wie allen Einflüssen resistent sind. Die Idee hinter diesen Probiotika stammt aus der Forschung gegen die Bekämpfung von pathogenen sporenbildenden Bakterien – also Krankheitserregern, die ebenfalls diese Sporenbildung als Fähigkeit besitzen. Weiterhin entdeckte Sporen untersucht, die zum Teil vor Tausenden von Jahren sporuliert waren (Sporulation beschreibt den Prozess der Sporenbildung).
Auch wenn Sporenbildner sehr resistent sind, gibt es auch zu ihnen Evidenz bezüglich deren Haltbarkeit1,2,3. Im Folgenden wollen wir Lactobazillen und Sporenbilder einmal gegenüberstellen:
| Umweltbedingung | Lactobacillen/Bifidobacterien | Bacillus-Arten (Sporenbildner) |
|---|---|---|
| Hitze (z. B. Kochen, Backen oder Pasteurisierung) | Diese Bakterien sind empfindlich – beim Erwärmen gehen viele verloren. Beispiel: Wenn Du Joghurt stark erhitzt, überleben nur wenige. | Sehr hitzestabil – fast alle überleben, auch längere Pasteurisierung. So bleiben sie auch nach warmer Verarbeitung aktiv. |
| Magensäure (natürliche Schutzbarriere gegen Keime) | Viele Bakterien werden sofort abgetötet, nur 10.000–100.000 überleben pro Kapsel. Beispiel: Nach Einnahme einer Kapsel erreichen nur ein kleiner Teil den Darm. | Sporen überstehen die Magensäure gut und gelangen lebend in den Darm, auch nach mehreren Stunden. |
| Lagerung über längere Zeit | Weniger stabil – ihre Zahl nimmt mit der Zeit ab. Beispiel: Joghurt oder Probiotika verlieren nach Monaten merklich an Wirksamkeit. | Langzeitstabil: Auch nach über 1,5 Jahren Lagerung bleibt eine große Menge lebendig. Produkte bleiben somit länger wirksam. |
| Gefriertrocknung (Herstellung) | Brauchen Schutzstoffe, damit sie den Prozess überleben. Beispiel: Pulverisierte Probiotika werden oft stabilisiert. | Sehr robust – überstehen Gefriertrocknung ohne große Verluste. |
Fazit: Sporenbildende Probiotika zeigen also unter den meisten Stressbedingungen konsistente und erhebliche Vorteile in der Überlebensfähigkeit im Vergleich zu nicht sporenbildenden Probiotika.
Die dramatischsten Unterschiede treten vermutlich unter Magensäurebedingungen auf, wo nicht sporenbildende Probiotika oft eine rasche Inaktivierung erfahren, während sporenbildende Stämme eine nahezu vollständige Lebensfähigkeit beibehalten.
Sporenbildner haben also eine besonders gute Haltbarkeit und Stabilität. Aber welche der vielen Bakterienarten, die Du auf der Inhaltsstoffliste lesen kannst, gehören denn zu den Sporenbildnern? Und haben diese untereinander auch Unterschiede? Das wollen wir uns jetzt anschauen.
Welche sporenbildenden Probiotika gibt es?
Kurzum gibt es besonders zwei sporenbildende Gattungen, die Du dir merken solltest: Die Bacillus- und die Clostridium-Gruppe. Vielleicht kennst du den Begriff Clostridien von Infektionserkrankungen? Tatsache ist nämlich, dass es unter den Sporenbildnern “positive” Arten gibt, die wir dann als Probiotika klassifizieren, zum Beispiel C. butyricum. Es gibt aber auch Krankheitserreger wie C. tetani (Tetanus) und C. botulinum. Auch bei der Bacillus-Gattung gibt es probiotische Arten: B. coagulans, B. subtilis und B. clausii (mehr zu diesen weiter unten.) Andere hingegen, wie etwa B. cereus, können Lebensmittelvergiftungen verursachen.
Dieser kleine Exkurs soll Dir zeigen, dass es durchaus darauf ankommt, von welchen Bakterien wir sprechen, da sie unterschiedliche Funktionen haben. Aber: Keine Angst vor Sporenbildnern als Probiotika – die klassischen probiotischen Arten haben keinen Krankheitswert. Gehen wir kurz auf die angesprochenen Bacillus-Arten an, die in der Probiotika-Welt am interessantesten sind:
-
Bacillus coagulans
Bacillus coagulans ist ein spezielles Probiotikum. Es ist nämlich nicht Teil der natürlichen Darmflora und siedelt sich auch nicht an – wie kann es dann überhaupt Effekte haben?
Sobald es im Dünndarm angekommen ist, kann sich die Spore “wiederbeleben” und das Bakterium sich vermehren. Wenn es wieder einen aktiven Stoffwechsel hat, produziert es Milchsäure. Diese wiederum hat einen positiven Effekt auf den pH und das generelle Milieu4 – ein Problem bei vielen SIBO- und Reizdarm-Patienten. Die Verbesserung des Milieus über weitere Stoffwechselprodukte kann außerdem den Gehalt an anderen hilfreichen Bakterien der Darmflora erhöhen. B. coagulans LBSC beispielsweise hat sich hilfreich bei der Behandlung des Reizdarmsyndroms erwiesen, da es Symptome wie Blähungen, Bauchschmerzen und Durchfälle signifikant vermindern konnte5.
Einige B. coagulans Stämme können auch Bakteriocine und bakteriocin-ähnliche Substanzen produzieren6. Das sind antimikrobielle Peptide, die das Wachstum und die Lebensfähigkeit pathogener Keime beeinträchtigen.
-
Bacillus subtilis
Eben solche antimikrobiellen Peptide werden auch von einigen Bacillus subtilis Stämmen produziert – diese sind bekannt für ihre kompetitive Verdrängung und Hemmung pathogener Keime7. Im Gegensatz zu B. coagulans ist B. subtilis Teil der Darmflora; zugeführte Sporen in Probiotika kolonisieren den Darm aber nicht8.
Neben der antimikrobiellen Aktivität werden ihnen viele weitere positive Effekte nachgesagt. So konnte in Bezug auf einige B. subtilis Stämme wie DE111 oder BS50 gezeigt werden, dass sie Blähungen reduzieren oder die Stuhlkonsistenz normalisieren konnten, sowie antiinflammatorische Effekte zeigten und protektiv auf die Darmbarriere wirkten.8 Inwiefern diese Effekte auf andere B. subtilis Stämme übertragen werden können, wird sich noch zeigen.
-
Bacillus clausii
B. clausii Stämme haben in der Vergangenheit besonders viel Anwendung in der Lebensmittelindustrie erfahren, da sie mit am widerstandsfähigsten sind. Etwas weniger Evidenz gibt es zur Nutzung im probiotischen Kontext, wobei besonders zu B. clausii die letzten Jahre das Interesse zugenommen hat. So gibt es Hinweise darauf, dass diesem Bakterium besonders immunmodulatorische Effekte zugeschrieben werden können – unter anderem aufgrund antimikrobieller Aktivität, ähnlich wie bei anderen Bacillus-Arten, aber auch aufgrund immunstimulierender Effekte aufgrund seiner Oberfläche9.
In Studien mit Kindern und Erwachsenen mit Heuschnupfen (allergische Rhinitis) konnte gezeigt werden, dass B. clausii das Immunsystem in eine günstigere Richtung unterstützt10. Normalerweise ist bei Heuschnupfen ein Ungleichgewicht im Immunsystem vorhanden, das bestimmte Abwehrstoffe (sogenannte Zytokine) stärker aktiviert. Die Einnahme von B. clausii kann helfen, dieses Gleichgewicht wiederherzustellen. Außerdem wird B. clausii häufig eingesetzt, um die Beschwerden während einer Behandlung mit Antibiotika gegen Helicobacter pylori11 zu lindern, sowie zur Verhinderung anderer antibiotika-assoziierter Diarrhö12.
Jetzt weißt Du schon etwas mehr über einzelne Stämme. Fassen wir die Effekte sporenbildender Probiotika nochmals zusammen.
Wie helfen sporenbildende Probiotika Deinem Darm?
Sporenbildende Probiotika wie B. coagulans, B. subtilis und B. clausii wirken über mehrere, sich ergänzende Mechanismen – und genau das macht sie besonders interessant.
Ihr entscheidender Vorteil gegenüber klassischen Probiotika beginnt bereits vor dem Darm: Dank ihrer Sporenstruktur überstehen sie Magensäure, Hitze und Lagerung weitgehend unbeschadet und erreichen den Dünndarm in deutlich höherer Anzahl als viele nicht sporenbildende Stämme. Dort angekommen, keimen sie aus und entfalten ihre Wirkung transient, was gerade für SIBO-Patienten interessant ist.
Im Darm selbst greifen mehrere Wirkmechanismen ineinander:
- Milieuverbesserung: B. coagulans produziert Milchsäure und beeinflusst so den pH-Wert im Darm positiv – was besonders bei Reizdarm und SIBO relevant ist
- Antimikrobielle Aktivität: Bacillus-Arten produzieren Bakteriocine und antimikrobielle Lipopeptide, die pathogene Keime hemmen und so das Gleichgewicht der Darmflora stabilisieren
- Barriereschutz: Klinische Studien mit Bacillus-Sporenmischungen zeigten beim Menschen in einer kleineren Studie eine Reduktion der sogenannten metabolischen Endotoxämie – also der Menge an bakteriellen “Giftstoffen” (Lipopolysaccharide), die nach dem Essen ins Blut übertreten – um bis zu 42%13; das deutet auf eine Stärkung der Darmbarriere hin, die bei Reizdarm oft beeinträchtigt ist
- Immunmodulation: B. clausii beeinflusst das Zytokinprofil – z. B. durch eine Verschiebung in Richtung Th1-Immunantwort und Reduktion proinflammatorischer Zytokine wie IL-1β und IL-12
- Symptomkontrolle bei Reizdarm und funktionellen Beschwerden: Mehrere randomisierte, kontrollierte Studien zeigten signifikante Verbesserungen von Bauchschmerzen, Blähungen und Stuhlkonsistenz – sowohl bei Durchfall- als auch bei Verstopfungs-betontem Reizdarm
- Unterstützung bei Antibiotikaeinnahme: Speziell B. clausii zeigte eine signifikante Reduktion antibiotika-assoziierter Durchfälle (AAD)
Zusammenfassung
Soviel auch über Probiotika und Sporenbilder mittlerweile bekannt ist – und wir hoffen Dir mit diesem und unseren weiteren Artikeln einen hilfreichen Einblick zu verschaffen – eine Menge an Fragen sind noch nicht geklärt. Das Forschungsgebiet zu sporenbildenden Bakterien als Probiotika ist nämlich nach wie vor jung. Bis dahin können wir aber schon mit der bisherigen Evidenz arbeiten: Es gibt bereits Stämme, die von Lebensmittelbehörden auf Sicherheit geprüft wurden und positive Erfahrungsberichte sowie klinische Studien besonders beim Reizdarmsyndrom, Durchfall sowie der antimikrobiellen Aktivität und der Verbesserung des Darmmilieus. Letztere beiden Aspekte können besonders im Kontext SIBO (Dünndarmfehlbesiedlung) hilfreich sein.
Referenzen (Englisch)
- Majeed, M., Majeed, S., Arumugam, S., Ali, F., & Beede, K. (2021). Comparative evaluation for thermostability and gastrointestinal survival of probiotic Bacillus coagulans MTCC 5856. Bioscience, biotechnology, and biochemistry, 85(4), 962–971. https://doi.org/10.1093/bbb/zbaa116
- Fajardo-Cavazos, P., & Nicholson, W. L. (2021). Shelf Life and Simulated Gastrointestinal Tract Survival of Selected Commercial Probiotics During a Simulated Round-Trip Journey to Mars. Frontiers in microbiology, 12, 748950. https://doi.org/10.3389/fmicb.2021.748950
- Brachkova, M. I., Duarte, A., & Pinto, J. F. (2009). Evaluation of the viability of Lactobacillus spp. after the production of different solid dosage forms. Journal of pharmaceutical sciences, 98(9), 3329–3339. https://doi.org/10.1002/jps.21609
- Payne, J., Bellmer, D., Jadeja, R., & Muriana, P. (2024). The Potential of Bacillus Species as Probiotics in the Food Industry: A Review. Foods (Basel, Switzerland), 13(15), 2444. https://doi.org/10.3390/foods13152444
- Gupta, A. K., & Maity, C. (2021). Efficacy and safety of Bacillus coagulans LBSC in irritable bowel syndrome: A prospective, interventional, randomized, double-blind, placebo-controlled clinical study [CONSORT Compliant]. Medicine, 100(3), e23641. https://doi.org/10.1097/MD.0000000000023641
- Honda, H., Gibson, G. R., Farmer, S., Keller, D., & McCartney, A. L. (2011). Use of a continuous culture fermentation system to investigate the effect of GanedenBC30 (Bacillus coagulans GBI-30, 6086) supplementation on pathogen survival in the human gut microbiota. Anaerobe, 17(1), 36–42. https://doi.org/10.1016/j.anaerobe.2010.12.006
- Khochamit, N., Siripornadulsil, S., Sukon, P., & Siripornadulsil, W. (2015). Antibacterial activity and genotypic-phenotypic characteristics of bacteriocin-producing Bacillus subtilis KKU213: potential as a probiotic strain. Microbiological research, 170, 36–50. https://doi.org/10.1016/j.micres.2014.09.004
- Williams, N., & Weir, T. L. (2024). Spore-Based Probiotic Bacillus subtilis: Current Applications in Humans and Future Perspectives. Fermentation, 10(2), 78. https://doi.org/10.3390/fermentation10020078
- Villéger, R., Saad, N., Grenier, K., Falourd, X., Foucat, L., Urdaci, M. C., Bressollier, P., & Ouk, T. S. (2014). Characterization of lipoteichoic acid structures from three probiotic Bacillus strains: involvement of D-alanine in their biological activity. Antonie van Leeuwenhoek, 106(4), 693–706. https://doi.org/10.1007/s10482-014-0239-8
- Wong-Chew, R. M., de Castro, J. A., Morelli, L., Perez, M., & Ozen, M. (2022). Gut immune homeostasis: the immunomodulatory role of Bacillus clausii, from basic to clinical evidence. Expert review of clinical immunology, 18(7), 717–729. https://doi.org/10.1080/1744666X.2022.2085559
- Nista, E. C., Candelli, M., Cremonini, F., Cazzato, I. A., Zocco, M. A., Franceschi, F., Cammarota, G., Gasbarrini, G., & Gasbarrini, A. (2004). Bacillus clausii therapy to reduce side-effects of anti-Helicobacter pylori treatment: randomized, double-blind, placebo controlled trial. Alimentary pharmacology & therapeutics, 20(10), 1181–1188. https://doi.org/10.1111/j.1365-2036.2004.02274.x
- Abreu, A. T., Vázquez Frías, R., Boggio Marzet, C., Stefanolo, J. P., Concha Mejía, A., Bustos Fernández, L., Laudanno, O., Rosa, D., Cruz Serrano, M. C., Cárdenas, K., & Zuluaga, J. (2025). Effectiveness of Bacillus clausii (O/C, N/R, SIN, T) in the Prevention of Antibiotic-Associated Diarrhea and Gastrointestinal Symptoms: A Systematic Review. Antibiotics (Basel, Switzerland), 14(5), 439. https://doi.org/10.3390/antibiotics14050439
- McFarlin, B. K., Henning, A. L., Bowman, E. M., Gary, M. A., & Carbajal, K. M. (2017). Oral spore-based probiotic supplementation was associated with reduced incidence of post-prandial dietary endotoxin, triglycerides, and disease risk biomarkers. World journal of gastrointestinal pathophysiology, 8(3), 117–126. https://doi.org/10.4291/wjgp.v8.i3.117